RICOMINCIAMO IN SICUREZZA
Il Centro Oculistico Quattroelle è nuovamente operativo nel rispetto di tutte le norme di sicurezza necessarie.
Il Personale Medico e di Assistenza è provvisto di adeguati dispositivi di protezione personale e procede regolarmente con la disinfezione di tutto il materiale diagnostico prima e dopo ogni visita.
Un comportamento corretto e rispettoso dei pazienti e del personale è fondamentale per accedere serenamente ed in sicurezza alle prestazioni.
Degenerazione maculare senile
Cura per la degenerazione maculare senile
ACCORGIMENTI: La prevenzione, ovvero la possibilità di ritardare la progressione della degenerazione maculare senile, va attuata precocemente, quando ancora la situazione clinica e funzionale è buona.
All’uopo si prescrivono lenti (negli operati di cataratta si impiantano cristallini artificiali speciali) che proteggono dai raggi ultravioletti e dalla luce blu, evitando gli ambienti particolarmente assolati; vanno corretti i fattori di rischio generali come il fumo, l’alimentazione, lo stile di vita sedentario e l’ipertensione.
Nella miscela più moderna di integratori della dieta (vitamina A,C,E, antiossidanti come lo zinco, il selenio, la luteina e la zeaxantina, acidi grassi omega 3) non compare più il betacarotene (chi non ricorda i benefici della carota?), dato il rischio di favorire il cancro polmonare nei fumatori. Le conferme allo studio americano (il famoso AREDS) che ne avrebbe dimostrato l’efficacia, non sono però unanimi, e, anche se ‘male non fanno’, la notevole spinta commerciale giustifica più di un dubbio sul rapporto costo/beneficio di tali prodotti.
In ogni caso un’alimentazione ‘sana’, ricca di principi attivi (vegetali a foglia verde come spinaci, cavoli, cime di rapa, frutta fresca, pesce azzurro ricco di omega-3, vino rosso di qualità…) e povera di carboidrati raffinati (dolci), combinata a un regolare esercizio fisico è assolutamente consigliabile.
In attesa della disponibilità di innovative cure geniche o di trapianto di cellule staminali, per le quali è lecito attendersi significativi miglioramenti nei prossimi decenni, la terapia della degenerazione maculare senile essudativa si avvale delle seguenti opzioni:
LASER e TERAPIA FOTODINAMICA (PDT)
La fotocoagulazione laser diretta delle lesioni è applicabile soltanto in casi rari e ben selezionati (neovascolarizzazioni distanti dal centro della macula, individuazione del vaso afferente o feeder vessel), dato che l’inevitabile conseguenza della cicatrizzazione delle aree retiniche viciniore comporta di per sé un danno alla visione.
Con la terapia fotodinamica (PDT: PhotoDynamic Therapy), introdotta agli inizi del 2000, un laser a bassa intensità attiva un farmaco fotosensibilizzante (la verteporfina, o Visudyne®) che, iniettato endovena, si lega a determinati recettori dell’endotelio vascolare.
L’obiettivo è la chiusura selettiva dei neovasi coroideali senza provocare danno alle strutture vicine, così come avviene con il laser convenzionale. Nonostante un eccellente profilo di sicurezza (gli unici effetti collaterali sono rappresentati dalle reazioni allo stravaso del liquido dalla vena, dal dolore alla schiena, peraltro di origine non chiara, e dalla necessità di non esporsi alla luce solare per 24 ore onde evitare reazioni di fotosensibilizzazione), buona parte delle aspettative di efficacia nel lungo periodo sono andate deluse.
Oggi viene utilizzata per lo più in combinazione con i farmaci anti-VEGF e soprattutto nelle neovascolarizzazioni sottoretiniche che complicano la miopia elevata.
INIEZIONE INTRAVITREALE di FARMACI ANTI-ANGIOGENETICI
L’angiogenesi (crescita di vasi sanguigni) è un processo fisiologico, dinamico e molto complesso, tuttora poco noto, regolato da un gran numero di fattori pro e antiangiogenetici, in cui il VEGF (fattore di crescita endoteliale vascolare, Vascular Endothelial Growth Factor) e i suoi recettori giocano un ruolo fondamentale.
Il VEGF agisce attraverso diversi meccanismi d’azione ed è stato identificato a livello intraoculare in tutte le patologie oculari sopra elencate. Gli Anti-VEGF sono molecole che bloccano o inibiscono il VEGF, aiutano cioè a prevenire l’ulteriore crescita dei vasi sanguigni anomali e a ridurre l’alterazione della permeabilità dei vasi da cui proviene l’edema delle strutture oculari e i conseguenti disturbi visivi.
Dopo la dilatazione pupillare e l’anestesia dell’occhio mediante gocce, il farmaco anti-VEGF viene iniettato nel vitreo, la sostanza gelatinosa che riempie la camera posteriore del bulbo oculare (Figura 6).
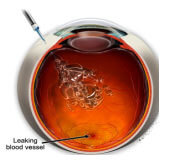
Figura 6. Iniezione intravitreale di farmaci anti-VEGF.
L’AVASTIN® (bevacizumab) un anticorpo monoclonale “umanizzato”, in modo da evitare la risposta del sistema immunitario è stato il precursore della terapia anti-VEGF. Inizialmente sviluppato per la terapia del cancro del colon-retto metastatico per il quale è stato registrato in Europa ha mostrato in modo casulae la sua efficacia nella DMS, l’osservazione casuale della sua efficacia nella DMS ha fatto da apri-pista all’utilizzo oculistico degli anti-VEGF.
Per anni è stato utilizzato come “off-label”, ossia al di fuori delle indicazioni riportate sulla scheda tecnica autorizzata, in quanto non vi erano alternative valide alla sua efficacia verificata in tutto il mondo. Il ricorso a pratiche e farmaci off-label è non solo autorizzato dalla legge, ma molto comune nella pratica clinica, ad esempio in pediatria. Il suo largo utilizzo inoltre è stato convalidato da vari studi che hanno dimostrato la sua efficacia e per il suo basso costo si è diffuso rapitamente per la cura farmacologica della DMS.
Dall’avvento dell’Avastin nella cura della degenerazione maculare senile si sono poi susseguite altre molecole che sono attualmente in commercio: Lucentis, Macugen e Eylea
Il LUCENTIS® (ranibizumab) è un frammento anticorpale umanizzato derivato dall’Avastin, che blocca tutte le forme di VEGF (VEGF165, VEGF121, and VEGF110). Rispetto all’Avastin, Lucentis è stato progettato per l’occhio, è una molecola più piccola e ha una maggior capacità di penetrare tutti gli strati della retina e nello spazio sottoretinico.
Diversi studi hanno dimostrato l’efficacia del Lucentis nel mantenimento dell’acuità visiva e in alcuni casi nell miglioramento del’acuità visiva, dimostrando maggiori risultati rispetto alla PDT o a gruppi di controllo con Placebo. La permanenza del Farmaco in camera vitrea è di 1 mese e generalemente si esegue una dose di attacco con un ciclo di 3 iniezioni una a distanza di un mese una dall’altra e poi caso per caso si valuta l’eventuale ritrattamento.
L’ EYLEA (Aflibercept), è l’unica proteina di fusione completamente umana, che legandosi alle isoforme del VEGF-A ,VEGF-B e del Fattore di Crescita Placentare (PlGF) esegue la sua azione antiangiogenetica a livello retinico per contrastare la DMS grazie al suo particolare meccanismo d’azione che consente la sua adesione e l’intrappolamento del VEGF.
Eylea ha dimostrato la sua efficacia in particolare la sua non inferiorità rispetto al Lucentis e la sua efficacia per ben 2 mesi nel mantenimento dell’acuità visiva, il doppio del tempo rispetto al suo predecessore Lucentis ed inoltre il suo utilizzo è risultato efficace anche nell’edema maculare diabetico.
Il MACUGEN® (pegaptanib) è un aptamero, vale a dire un piccolo frammento di RNA sintetico, con conformazione tridimensionale e altamente specifica, che si lega ad uno specifico recettore (per il VEGF165). Si utilizza solitamente per quei pazienti che hanno dei problemi di salute generale quali una storia di eventi ischemici sistemici che controindicano l’utilizzo del Lucentis o dell’Eylea .
I trattamenti farmacologici con le iniezioni intravitreali di anti-VEGF hanno un effetto limitato nel tempo, legato alla permanenza della sostanza all’interno della cavità vitrea. I vari studi clinici danno delle linee guida sulla posologia dei trattamenti delle iniezioni, ma la sua risposta viene valutata caso per caso consentendo di poter eseguire una terapia mirata ad ottenere i migliori risultati possibili in termini di mantenimento della visione centrale.
La tempestività e la corretta esecuzione dei trattamenti sono fondamentali per la cura della degenerazione maculare senile, se invece si perde tempo prezioso si rischia un pregressivo e irreversibile danno maculare con conseguente perdita della visione distinta delle immagini.
Il futuro
Oltre un centinaio di terapie innovative sono in fase sperimentale e saranno disponibili nei prossimi anni. Per la tanto negletta degenerazione secca si sta studiando il Lampalizumab una molecola che inibisce il fattore D nella via del complemento, molecola che sembra faccia diminuire l’atrofia a livello maculare e porterebbe a un rallentamento della progressione degenerativa.
Altre speranze si chiamano fenretinide, ACU-4429, AL-8309B, sirolimus, POT-4 e OT-551, farmaci capaci di limitare l’accumulo di un detrito cellulare tossico nell’epitelio pigmentato retinico chiamato lipofuscina. Un discorso a parte meritano i vari fattori neurotrofici (come il CNTF) e rigenerativi (come l’oncomodulina), studiati per il trattamento di malattie degenerative del sistema nervoso.
Altre Opzioni
In casi particolari, le terapie citate possono essere variamente combinate tra loro al di fuori dagli schemi prestabiliti. Inoltre l’utilizzo di steroidi (cortisonici) come ad esempio il triamcinolone, iniettati nel vitreo o attorno al bulbo (peribulbare) o utilizzati per via sistemica può rispondere a un criterio razionale nei casi in cui si associa una componente infiammatoria.
Numerosi altre sostanze e procedure sono in fase di sperimentazione più o meno avanzata. Citiamo ad esempio l’uso di anti-VEGF in collirio, la Retinal Regenerative Therapy con il laser, la reoferesi, un tipo di filtrazione del sangue che rimuove le sostanze circolanti associate con la DMS (colesterolo LDL, anticorpi anti-IgM e altre) per migliorare la microcircolazione retinica. Uno spazio particolare merita la brachiterapia strontium-90, un’irradiazione con radiazioni beta (la dose è inferiore a quella ricevuta in una lastra del torace) effettuata in combinazione con una vitrectomia standard, che avrebbe il vantaggio, in paragone con le iniezioni di anti-VEGF, di essere effettuata una sola volta. I dati, assai promettenti, sono in fase finale di valutazione; le complicazioni sono collegate all’aspetto chirurgico e non gravi (la più frequente, l’induzione di cataratta).
La CHIRURGIA ha poco spazio nella degenerazione maculare senile. La rimozione della membrana neovascolare attraverso l’ingresso con pinza nello spazio sottoretinico, infatti, conduce inevitabilmente ad una cicatrice che tende a ingrandirsi negli anni e non ha mostrato benefici significativi se non in casi rari, in cui la membrana neovascolare è lontana dalla fovea.
La traslocazione maculare sposta la zona maculare ricollocandola su un’area di coroide non malata. Si tratta di una procedura complessa e traumatica, gravata da un alto tasso di complicanze, dato che disinserisce la retina e la ruota, oltre a spostare i muscoli oculo-motori per evitare la percezione di un mondo inclinato.
Le retine artificiali, microchip da inserire al posto della retina per convertire i segnali luminosi in stimolazioni appropriate alle residue cellule retiniche, sono per ora una opzione futuribile in corso di sperimentazione e che si spera portino a dei risultati incoraggianti.
I telescopi miniaturizzati impiantabili (Figura 7) utilizzano gli stessi principi di ingrandimento descritti nei presidi per ipovedenti. Come per l’adozione di questi ultimi, un ciclo completo di rieducazione specializzata deve accompagnare l’intervento, poco più complesso di quello per la cataratta.
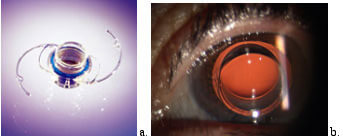
Figura 7. Impianto telescopico miniaturizzato fuori (a) e dentro l’occhio (b).
Nella forma più frequente (la cosiddetta ‘prevalentemente classica’) le lesioni interessano la fovea; i sintomi esordiscono in maniera improvvisa ed evolvono in maniera rapida e aggressiva, con gravi ripercussioni funzionali. In base all’aspetto fluorangiografico, si classificano poi:
- lesioni ‘classiche’, membrane dai margini ben definiti durante le fasi iniziali, con diffusione del colorante attorno e nello spazio sottoretinico entro 2-3 minuti dall’iniezione, a sede sottofoveale, oppure extra (oltre 200 µm) o juxtafoveale (meno di 200 µm dal centro della zona foveale avascolare);
- lesioni ‘occulte’, in quanto nascoste e non ben definite dal quadro fluorangiografico;
- forme miste, ‘prevalentemente’ (componente classica >50% della lesione) o ‘minimamente classiche’ (componente classica <50% della lesione).
In ogni caso, la membrana neovascolare tende ad estendersi sino alla formazione di una cicatrice fibrosa che sovverte in maniera anche drammatica l’organizzazione anatomica e funzionale della retina centrale. La perdita di funzione visiva è sovente completa.
Nelle fasi iniziali la sintomatologia è rappresentata dalla visione centrale distorta (metamorfopsie) o confusa, appannamento e alterazione dei colori (discromatopsia) e/o da scotomi positivi (comparsa di macchie scure fisse) che possono essere ben evidenziate con lo schermo di Amsler o test della griglia (Figura 4).
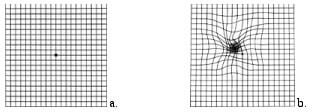
Figura 4. Normalità (a) e distorsioni (b) individuate dal test di Amsler.
L’angiografia con fluoresceina e con verde d’indocianina e l’OCT maculare sono gli esami fondamentali nella degenerazione maculare senile (Figura 5) per stabilire una diagnosi precisa e quindi una terapia ed una prognosi appropriata.
Una volta raggiunto lo stadio avanzato, nessun trattamento può far recuperare la vista nella DMS secca.
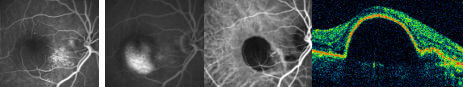
Figura 5. Quadro fluorangiografico precoce (a), tardivo (b), indocianinografico (c) e OCT (d) di una DMS essudativa.
Cos’è la degenerazione maculare senile?
Nei paesi industrializzati, la degenerazione maculare senile (DMS) è la più comune causa di cecità legale nei pazienti che hanno la ‘fortuna’ di invecchiare oltre i 60 anni di età.
La sua incidenza è destinata ad esplodere nei prossimi anni, considerato l’invecchiamento medio della popolazione. Si tratta di una malattia della macula, in cui le cellule più raffinate del sistema visivo vanno in progressiva sofferenza (degenerano) e alla fine muoiono, sostituite da tessuto cicatriziale privo di dotazione funzionale.
La visione centrale si spegne; pur comprendendo non più del 5% della superficie retinica, la macula è responsabile di più del 35% del campo visivo, per cui la degenerazione maculare senile grave rende difficile, se non impossibile, guidare la macchina, leggere, distinguere i visi delle persone.
La visione periferica, tuttavia, è intatta e non è a rischio. La DMS non provoca quindi la cecità completa ed è possibile tornare a svolgere determinate occupazioni in maniera indipendente e produttiva ricorrendo ai presidi e alle tecniche di riabilitazione per ipovedenti.
La rieducazione visiva della degenerazione maculare senile si avvale di accorgimenti (come le lampade alogene, da preferire a quelle a bulbo), strumenti ingrandenti, televisori a circuito chiuso, speciali sistemi telescopici, anche inseribili all’interno dell’occhio e di una serie di tecniche di apprendimento e adattamento ambientale, per sfruttare al massimo la potenzialità residua della retina periferica.
La DMS è una malattia complessa, multifattoriale, in cui alterazioni microcircolatorie isolate dello strato capillare che sta sotto la retina (la coriocapillare) innescano un meccanismo di degenerazione dell’epitelio pigmentato e degli strati esterni della retina, coinvolgendo i fotorecettori maculari (i coni).
Siccome esistono forme eredo-familiari di degenerazione maculare a carico di soggetti giovani (come nella miopia degenerativa, nelle strie angioidi, nelle malattie di Best, di Stargardt, di Sorsby…), oltre al trascorrere delle primavere, lo studio delle cause della degenerazione maculare senile si rivolge ad un mix di fattori genetici e ambientali, come il fumo di sigaretta, gli stili di vita incongrui (sedentarietà, dieta ricca di carboidrati raffinati e povera di proteine, vitamine, oligoelementi anti-ossidanti e acidi grassi poliinsaturi omega-3), l’ipertensione arteriosa, l’iperlipidemia, l’ipercolesterolemia, l’uso di taluni farmaci usati in reumatologia (la clorochina) o in psichiatria (i fenotiazinici), l’ipermetropia, i precedenti di infezione polmonare e l’esposizione prolungata alla luce solare intensa (ultravioletto).
Si distinguono classicamente due tipi principali di DMS, la forma secca o atrofica e la forma umida, anche detta essudativa o neovascolare.
Degenerazione maculare senile secca
Due situazioni anatomiche, tra loro variamente combinate caratterizzano la forma secca, la più frequente tipologia di DMS:
- le drusen, o corpi colloidi, depositi giallastri rotondeggianti, costituiti dall’accumulo sotto la retina di detriti, rifiuti o prodotti non perfettamente smaltiti dal metabolismo dell’epitelio pigmentato retinico. Si distinguono drusen ‘dure’, piccole, a margini netti che, insieme a chiazzette di atrofia possono restare asintomatiche per anni e drusen ‘soffici’, più grandi e a margini non ben definiti, che tendono a confluire ed a diventare più grandi (Figura 1), evolvendo verso gli stadi più avanzati sia della forma atrofica che di quella essudativa;
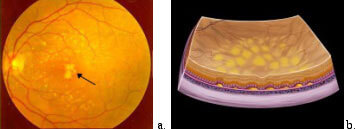
Figura 1. Drusen soffici della macula, indicate dalla freccia all’osservazione del fondo dell’occhio (a.) e in sezione (b.)
- le chiazze ‘a carta geografica’, lesioni areolari chiare di assottigliamento atrofico degli strati pigmentati della retina centrale, che lasciano intravedere i grossi vasi sottostanti tendono pian piano a ingrandirsi ed a confluire fino ad assumere una forma circolare, ovale o policiclica con margini più regolari (Figura 2).
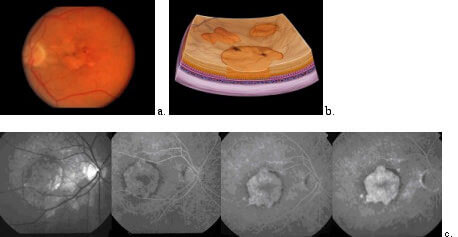
Figura 2. Immagini al fundus (a.), in sezione (b.) e angiografiche successive (c.) di lesioni atrofiche a carta geografica.
Anche se in generale l’evoluzione è molto lenta, la compromissione del visus è irreversibile e passa attraverso fasi intermedie con annebbiamento e distorsione delle immagini, perdita di contrasto con necessità di utilizzare forti ingrandimenti e illuminazioni per la lettura, percezioni di piccole zone cieche (scotomi), sino ad arrivare, negli stadi più avanzati, a deficit gravi, in cui il paziente riesce a mala pena a contare le dita della mano a pochi centimetri di distanza.
Degenerazione maculare senile essudativa
Circa il 15% dei casi di degenerazione maculare senile si presenta con la variante ‘umida’, caratterizzata dalla formazione di nuovi vasi a partenza dalla coroide, lo strato vascolare sottostante la retina (neovascolarizzazione o membrana neovascolare sottoretinica), più o meno associata ad un distacco sieroso dell’epitelio pigmentato retinico.
La fragilità e l’immaturità dei neovasi coroideali provoca le lesioni, fuoriuscite di siero e sangue più o meno importanti che deformano il piano retinico e alterano gli scambi metabolici (Figura 3).
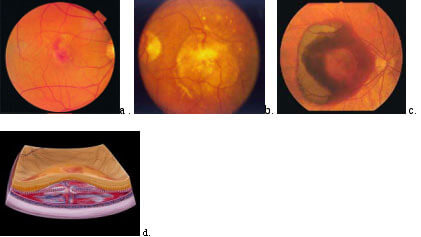
Figura 3. Tre casi di DMS neovascolare, iniziale (a), evoluta a carattere prevalentemente essudativo (b) e prevalentemente emorragico (c) all’osservazione del fondo. L’aspetto in sezione è mostrato in d.

